Статья переведена с английского языка.
Filipendula ulmaria (F. ulmaria) — та́волга вязоли́стная или лаба́зник вязоли́стный.
Alnus glutinosa (A. glutinosa) — Ольха́ чёрная, или Ольха европе́йская.
Скачать оригинал
1. Введение
В последние десятилетия мы наблюдаем стремительный рост числа пожилых и старых людей, что свидетельствует о глобальном старении населения. По прогнозам Организации Объединённых Наций (ООН), к 2025 году количество людей старше 60 лет превысит 1 миллиард.
Одной из ключевых задач современной профилактической медицины является увеличение продолжительности жизни человека, снижение заболеваемости и предотвращение преждевременного старения. Старение населения сопровождается ростом числа различных заболеваний, среди которых особое место занимают атеросклероз, ишемическая болезнь сердца, артериальная гипертензия, хроническая сердечная недостаточность и сахарный диабет.
Сердечно-сосудистая система первой подвергается возрастным изменениям, когда другие системы организма ещё сохраняют свою функциональность. Именно сердечно-сосудистая система во многом определяет, будет ли человек жить долго и активно или столкнётся с ранней старостью. Эти возрастные изменения тесно связаны с увеличением выработки активных форм кислорода (АФК) и развитием хронического окислительного стресса. Однако начало заболевания можно значительно отсрочить, если ежедневно употреблять натуральные растительные продукты, богатые антиоксидантами.
Сегодня эта стратегия признана одним из ключевых способов борьбы с преждевременным старением [3, 4]. Поэтому поиск новых источников природных антиоксидантов, способных предотвратить возрастные изменения в организме человека, становится всё более актуальным [5].
Эти антиоксиданты могут быть добавлены в функциональные продукты питания — диетические добавки, которые можно включить в ежедневный рацион для продления активной жизни и отсрочки старения. Они могут быть представлены в виде растительных экстрактов, биологически активных комплексов или отдельных соединений.. Таким образом, применение широко распространённых и, следовательно, легкодоступных лекарственных растений может значительно повысить экономическую эффективность этой стратегии и сделать функциональные продукты питания, богатые антиоксидантами, более доступными.
Антиоксиданты, используемые в диетическом питании и в медицине, в основном получают из сельскохозяйственных и лекарственных растений [6, 7]. Кроме того, важным источником природных антиоксидантов может быть промышленность, занимающаяся переработкой сельскохозяйственных отходов [8].
Природные антиоксиданты, содержащиеся в растительном сырье, включают полифенолы (такие как фенольные кислоты, флавоноиды, антоцианы, лигнаны и стильбены), каротиноиды (например, лютеин и каротин) и витамины (например, витамины E и C) [9]. Они обладают множеством биологических свойств, включая противовоспалительные, антибактериальные, противовирусные, антивозрастные и противораковые эффекты [10–15]. Значимость антиоксидантов для здоровья объясняет растущий интерес в сфере питания к практическим методам извлечения природных антиоксидантов, а также к адекватным способам оценки их активности и поискам их источников в сельскохозяйственных и лекарственных растениях [16].
В этом контексте особый интерес представляют препараты из Filipendula ulmaria и Alnus glutinosa, широко распространенных в Восточной Прибалтике и издавна известных своими целебными свойствами [18, 19].
Возрастающий спрос на использование официальных видов лекарственных растений в качестве перспективных лекарственных средств [20] и нехватка соответствующего сырья в России обуславливают необходимость проведения предварительных исследований для выявления сходных по химическому составу видов. В этой связи фитохимическое изучение F. ulmaria и A. glutinosa, произрастающих в Калининградской области, становится важным направлением.
Фитохимическое изучение F. ulmaria и A. glutinosa представляет собой важное направление в этой области. В Калининградской области можно встретить таволгу (Filipendula glutinosa), многолетнее травянистое растение из семейства розоцветных. Род таволги насчитывает около 30 видов, некоторые из которых произрастают в России: в Западной и Восточной Сибири, в европейской части, на Южном Урале, в Башкирии, на Дальнем Востоке, в Верхнем Приднепровье, Волжско-Камском и Верхне-Волжском регионах.
Одним из наиболее распространённых видов является Filipendula ulmaria (L.) Maxim, который признан официальным растением во многих странах. Исследования показали, что F. ulmaria, произрастающий в Западной Сибири, содержит производные салициловой кислоты [17], 2-пирон-4,6-дикарбоновую кислоту [21], фенилпропаноиды [22], флавоноиды [23], дубильные вещества [24] и эфирные масла [25]. Фенольные компоненты являются активными соединениями, которые придают препаратам на основе F. ulmaria иммуностимулирующие [26], антимикробные [27], противоаллергические [28] и другие свойства.
В рамках исследования были изучены антиоксидантные свойства двух растений — F. ulmaria и A. glutinosa, которые растут в Калининградской области. Эта область находится на западной окраине Русской равнины и граничит на севере и востоке с Литвой, на юго-западе — с Польшей, а с запада омывается водами Балтийского моря и его пресноводных заливов — Куршского и Калининградского.
Климат Калининградской области характеризуется как умеренно-континентальный, что обусловлено влиянием воздушных масс, формирующихся в Атлантике и на континенте Евразия. Кроме того, немаловажную роль играет и географическое положение области на юго-восточном побережье Балтийского моря.
На территории Калининградской области произрастает 1436 видов дикорастущей флоры и 699 видов декоративной древесно-кустарниковой флоры. Это свидетельствует о высокой степени насыщенности видами на сравнительно небольшой площади — 15000 км². Однако количественные и качественные характеристики видов F. ulmaria и A. glutinosa, а также их антиоксидантная активность изучены недостаточно.
В связи с этим мы предположили, что экстракты, полученные из растений F. ulmaria и A. glutinosa, которые произрастают в Калининградской области, могут обладать высокой антиоксидантной активностью. Если наша гипотеза подтвердится, то Калининградская область может стать перспективным регионом для культивирования этих растений в фармацевтических целях.
Насколько нам известно, это первое исследование, посвященное изучению антиоксидантного потенциала этих растений. Мы провели анализ антиоксидантных свойств водных, водно-этанольных, метанольных и этилацетатных экстрактов, полученных из надземных частей F. ulmaria и A. glutinosa, которые были собраны в Калининградской области.
2. Результаты
2.1 Общий выход экстрактов
На первом этапе были проанализированы общие выходы экстрактов (Таблица 1). Полученные данные свидетельствуют о том, что экстракция этилацетатом дала относительно низкие результаты. Это означает, что из растительного материала удалось извлечь сравнительно небольшое количество гидрофобных метаболитов, несмотря на то, что оптимальные условия экстракции (температура, время и объем экстрагента) были определены на основе литературных источников [31].
Максимальный общий выход экстракта для A. glutinosa (шишки) был достигнут при использовании метанола. В случае с F. ulmaria (листья) наиболее эффективной оказалась экстракция 70% водным этанолом.
Таблица 1. Общий выход растительных экстрактов

2.2 Содержание фенольных соединений
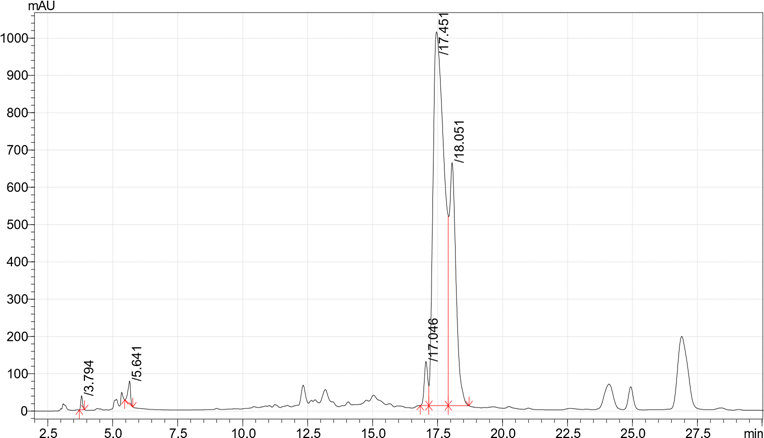
Исследование экстрактов F. ulmaria методом ОФ-ВЭЖХ показало высокое содержание фенольных соединений (Таблица 2, Рисунок 1). При этом 3,4-дигидроксибензойные кислоты и рутин были выявлены только в этилацетатном экстракте (Рисунок 1a), в то время как катехин — исключительно в метанольном экстракте (Рисунок 1b).
Кверцетин-3D-глюкозид, лютеолин-7-глюкозид, гиперозид и астрагалин были обнаружены во всех трех экстрактах F. ulmaria, при этом водно-этанольный экстракт содержал наибольшее количество этих веществ (Рисунок 1c). Галловая кислота также присутствовала во всех экстрактах, однако её концентрация была наиболее высокой в метанольном экстракте.
Таблица 2. Содержание отдельных фенольных соединений в экстрактах F. ulmaria и A. glutinosa
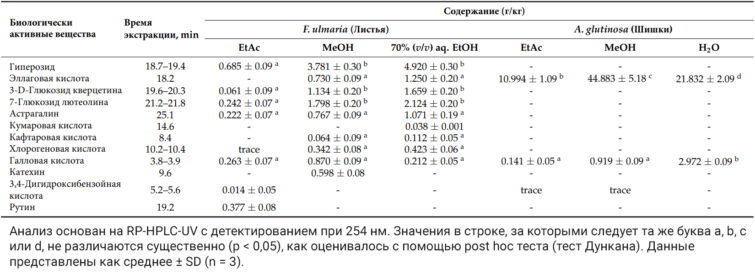
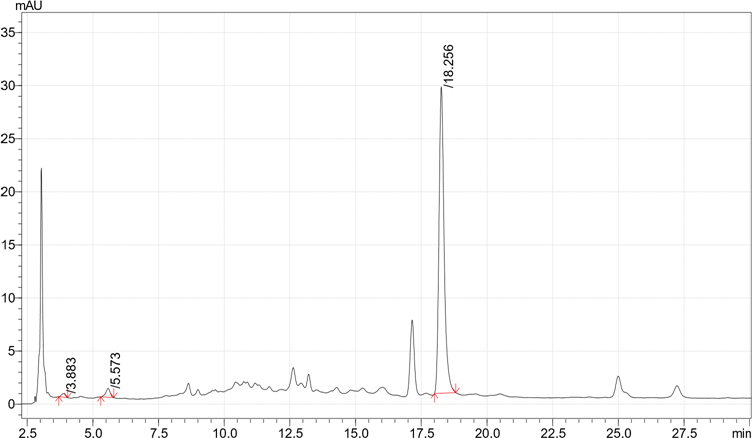
Рисунок 1. Хроматограммы ОФ-ВЭЖХ-УФ, полученные при 254 нм этилацетатных (a), метанольных (b) и водно-этанольных экстрактов (c) F. ulmaria (листья).
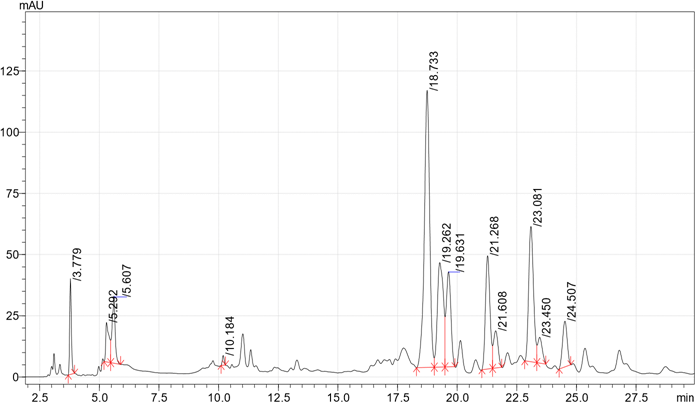
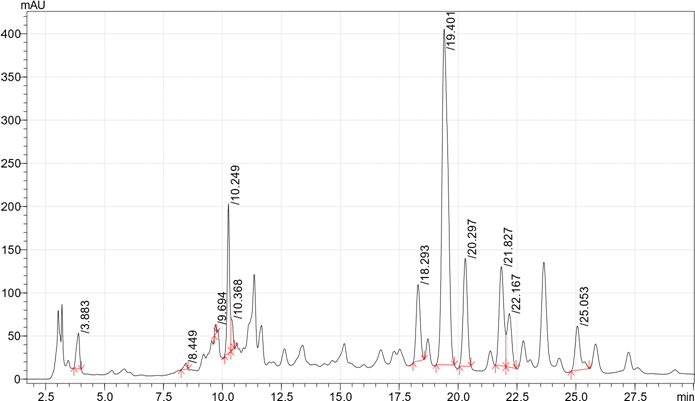
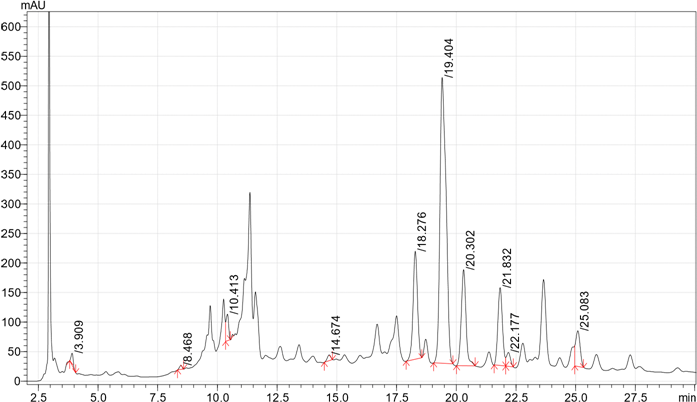
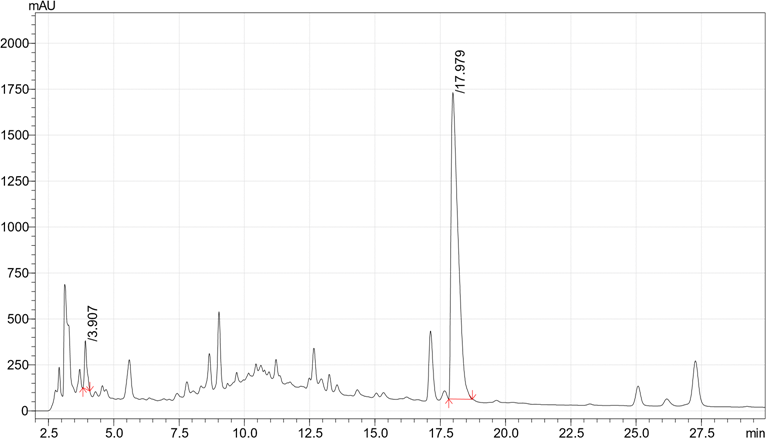
Экстракты A. glutinosa не обладали таким разнообразием фенольных соединений, как изоляты F. ulmaria (Таблица 1, Рисунок 2). Наиболее распространённым компонентом экстрактов шишек A. glutinosa являлась эллаговая кислота (Рисунок 2). Её содержание варьировалось от 10,994 до 44,883 г/кг (Таблица 1).
Кроме того, во всех экстрактах была обнаружена галловая кислота, а этилацетатные и метанольные экстракты содержали следовые количества 3,4-дигидроксибензойной кислоты.
В Таблице 2 представлено содержание фенольных соединений в экстрактах F. ulmaria и A. glutinosa.
Рисунок 2. Хроматограмма ВЭЖХ (a) этилацетата, (b) метанола (разбавление 1/100) и (c) водных экстрактов A. glutinosa (шишки).
2.3 Антиоксидантная активность экстрактов A. glutinosa и F. ulmaria
Для исследования антиоксидантной активности двух изучаемых растений мы выбрали несколько иную стратегию экстракции. Листья F. ulmaria были экстрагированы 70% (об.) водным этанольным раствором, этилацетатом и метанолом, в то время как для шишек A. glutinosa были использованы вода, этилацетат и метанол.
В нашем подходе мы опирались на исследование Раджбхара и его коллег [32], которые показали, что гидрофильные полифенолы, такие как флавоноидные агликоны и флавоноидные гликозиды, обладающие антиоксидантными свойствами, могут быть извлечены из растений с помощью воды, полярных органических растворителей, включая метанол, этанол, ацетонитрил и ацетон, или их водных смесей.
Из литературы известно, что эти соединения могут быть эффективно экстрагированы из жидких изолятов этилацетатом или водными смесями, в зависимости от их растворимости. В ходе предварительных испытаний было установлено, что антиоксидантные полифенолы F. ulmaria и A. glutinosa извлекаются с помощью выбранных растворителей. F. ulmaria, известная своими антиоксидантными свойствами, наиболее эффективно экстрагируется 70% (об.) водным раствором этанола, этилацетатом и метанолом. В то же время, полифенолы из A. glutinosa извлекаются водой, этилацетатом и метанолом.
Экстракты F. ulmaria, полученные с использованием различных органических растворителей, показали значительные различия (см. Таблицу 3). Метанольный экстракт продемонстрировал самую высокую антиоксидантную активность в улавливании радикалов ABTS и DPPH, а также самую высокую способность к восстановлению FRAP (759,78 ± 19,08 мкмоль TE/г, 451,08 ± 24,45 мкмоль TE/г и 332,28 ± 10,93 мкмоль TE/г соответственно). Экстракты F. ulmaria, полученные с использованием 70% (об.) водного этанольного раствора, также показали значительную антиоксидантную активность. Антиоксидантная активность этилацетатных экстрактов оказалась самой низкой среди трех изолятов.
Таблица 3. Антиоксидантная активность экстрактов, полученных из надземных частей F. ulmaria и A. glutinosa.
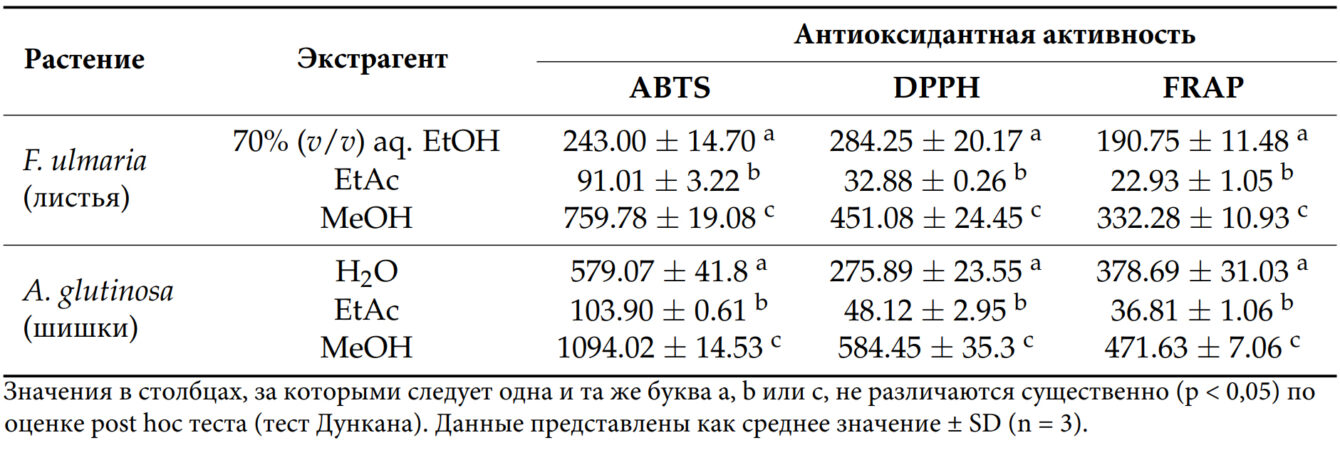
Как видно из Таблицы 3, метанольные экстракты A. glutinosa продемонстрировали самую высокую антиоксидантную активность, проявляющуюся в способности улавливать ABTS и DPPH радикалы, а также в восстановлении FRAP (1094,02 ± 14,53 мкмоль TE/г, 584,45 ± 35,3 мкмоль TE/г и 471,63 ± 7,06 мкмоль TE/г соответственно).
Этилацетатные экстракты A. glutinosa не показали значительных антиоксидантных свойств ни для одного из изолятов, их активность была минимальной, если не пренебрежимо малой.
3.Обсуждение
Исследования показали, что листья таволги вязолистной, которая широко распространена в различных регионах России, включая Самарскую область, содержат множество ароматических соединений. Среди них особенно выделяются фенилпропаноиды — спирты, альдегиды, кислоты и их производные [33–35].
Пыльца этого растения богата незаменимыми аминокислотами, тритерпеновыми кислотами, каротиноидами (бета-каротин), аскорбиновой кислотой, фенолкарбоновыми кислотами (хлорогеновые кислоты), а также флавоноидами, включая катехины.
Плоды таволги содержат дубильные вещества и флавоноиды, а семена — дубильные вещества, жирные масла и воск. Корневища и корни растения являются источником множества дубильных веществ, фенольных соединений, фенольных гликозидов, флавоноидов, фенольных кислот, кумаринов и витамина С [18, 36–39].
В проростках ольхи, произрастающей в лесостепной зоне Средней России, было обнаружено значительное количество стеролов, а также дубильных веществ и галловой кислоты [40]. Листья этого растения также содержат флавоноидные гликозиды, фенольные кислоты (бензоаты и фенилпропаноиды), пирокатехиновые кислоты и тритерпеноиды [40].
Ранее проведенные исследования подтвердили антиоксидантную активность изолятов, полученных из надземных частей F. ulmaria. Это свойство может быть объяснено относительно высоким содержанием флавоноидов, танинов, фенольных гликозидов (производных салицилатов), эфирных масел, минералов и витамина С в этом растении [41, 42]. Интересно, что высокое содержание полифенолов было обнаружено как в корнях, так и в листьях F. ulmaria [27, 43].
Это исследование и предыдущие работы показали, что в растениях Alnus glutinosa и Filipendula ulmaria, которые растут в разных регионах России, содержатся схожие вторичные метаболиты.
Наибольшее количество полифенолов и флавоноидов было обнаружено в метанольных экстрактах A. glutinosa и F. ulmaria, собранных в Калининградской области. Это свидетельствует о том, что метанольные экстракты этих растений обладают самой высокой антиоксидантной активностью.
В исследовании Дахии и его коллег [44] были изучены общие уровни фенольных кислот и флавоноидов, а также антиоксидантная активность метанольных экстрактов листьев и коры трёх видов ольхи.
Общее содержание фенолов в экстрактах определялось спектрофотометрическим методом Фолина–Чокальто. Антиоксидантная активность экстрактов оценивалась по способности поглощать радикал 1,1-дифенил-2-пикрилгидразила.
Результаты показали, что наибольшее количество общих фенолов содержится в экстракте коры A. glutinosa (780 мг CAT/г), в то время как экстракт листьев A. glutinosa содержит наибольшее количество флавоноидов (30,01 мг RUT/г). Все экстракты продемонстрировали более высокую антиоксидантную активность по сравнению с тимолом, который использовался в качестве положительного контроля.
Наши результаты согласуются с результатами предыдущих исследований [45]. В ходе изучения химического состава надземной части таволги вязолистной (F. ulmaria) было обнаружено [45], что она содержит широкий спектр веществ: простые фенолы, флавоноиды, органические кислоты, кумарины, дубильные вещества, антраценпроизводные, сапонины, полисахариды, каротиноиды, аминокислоты, а также макро- и микроэлементы.
В исследовании [46] было обнаружено, что водные и спиртовые экстракты надземной части таволги вязолистной демонстрируют высокую антиоксидантную активность в процессе электровосстановления кислорода. Все образцы активно взаимодействовали с активными формами кислорода.
Результаты показали, что антиоксидантная активность водно-этанольных экстрактов возрастает с увеличением концентрации этанола. Наиболее сильные антиоксидантные свойства проявились у 70% и 95% этанольных экстрактов.
Основываясь на этих данных, авторы провели более детальный анализ химического состава 70% водно-этанольного экстракта надземной части F. ulmaria. В ходе анализа было выявлено наличие следующих групп биологически активных веществ и индивидуальных соединений, которые были идентифицированы на основе их хроматографической подвижности по сравнению с эталонными образцами:
- простые фенолы, такие как рододендрол;
- флавоноиды, включая кверцетин, дигидрокверцетин, апигенин, изокверцитрин, гиперозид и рутин;
- органические кислоты, включая м-гидроксибензойную, салициловую, анисовую, бензойную, галловую, гентизиновую, феруловую, хлорогеновую, кофейную и хинную кислоты;
- кумарины, такие как эскулетин;
- гидролизуемые дубильные вещества;
- стероидные сапонины;
- аминокислоты.
Антиоксидантная активность растений обусловлена их уникальным составом, который включает множество различных антиоксидантов, особенно полифенольных соединений с уникальными механизмами действия [47]. Из-за их комплексного влияния на организм, для оценки антиоксидантной способности растительных экстрактов необходимо использовать несколько методов.
Наиболее распространёнными методами для определения антиоксидантной активности являются тесты на поглощательную способность DPPH и ABTS+. Эти тесты позволяют оценить способность различных активных фракций растений удалять свободные радикалы по сравнению с аскорбиновой кислотой (витамином С), которая используется в качестве контроля.
Среди всех активных компонентов, 2α,3β-дигидрокси-urs12-en-28-альдегид выделяется своей максимальной антиоксидантной активностью. Эта активность связана со структурой соединений типа урсана, которые присутствуют в составе исследуемых растений [47]. Другое объяснение заключается в том, что молекула с альдегидной группой более склонна к окислительным процессам, что, в свою очередь, приводит к более высокой антиоксидантной активности.
Предыдущие исследования подтвердили антиоксидантный потенциал различных экстрактов таволги. При оценке активности растений из родственных подродов было обнаружено, что сырые экстракты, полученные из разных источников, обладают высокой антиоксидантной активностью [47].
Антиоксидантная активность растений обусловлена их сложным составом, который включает разнообразные антиоксиданты, особенно полифенольные соединения с уникальными механизмами действия [47]. Из-за синергического взаимодействия этих компонентов, для оценки антиоксидантной способности растительных экстрактов необходимо применять несколько методов.
Наиболее часто используемыми методами для определения антиоксидантной активности являются оценка поглощающей способности DPPH и ABTS+. В ходе исследований, направленных на оценку способности различных активных фракций растений удалять свободные радикалы, были проведены эксперименты с DPPH и ABTS+, а также сравнительный анализ с аскорбиновой кислотой (витамином С), которая использовалась в качестве контроля.
По сравнению с другими активными компонентами, соединение 2α,3β-дигидрокси-urs12-en-28-альдегид продемонстрировал наилучшую антиоксидантную активность. Этот эффект, вероятно, обусловлен структурой соединений урсанового типа, присутствующих в исследуемых образцах [47]. Другое возможное объяснение заключается в том, что молекула с альдегидной группой более склонна к окислению и, следовательно, обладает более сильной антиоксидантной активностью.
Предыдущие исследования подтвердили антиоксидантный потенциал различных экстрактов таволги. При оценке активности растений из родственных подродов было обнаружено, что сырые экстракты, полученные из различных источников, обладают высокой антиоксидантной активностью [47].
Исследование Лаубертса и его коллег [48] показало, что фенольные соединения, извлечённые из A. glutinosa, содержат биоактивные компоненты, обладающие разнообразными полезными свойствами для здоровья человека. К ним относятся антиоксидантные, антибактериальные и противовоспалительные свойства.
В настоящее время A. glutinosa используется в основном как источник топлива, однако в статье [48] обсуждается его потенциал для производства биологически активных соединений. Большинство доступных методов экстракции требуют использования чистых органических растворителей для извлечения экстрактов с высоким антиоксидантным потенциалом из биомассы коры и шишек.
Однако, благодаря преимуществам ускоренной экстракции растворителем, было продемонстрировано, что использование деионизированной воды может стать альтернативой органическим растворителям.. В случае одностадийной водной экстракции общее содержание полифенолов в экстрактах варьировалось от 0,55 до 0,62 ГАЭ г/г в зависимости от температуры. При последовательной экстракции с использованием органических растворителей количество полифенолов в 40% этанольных экстрактах изменялось от 0,39 до 0,61 ГАЭ г/г, также в зависимости от температуры.
Было выявлено влияние общего содержания полифенолов и проантоцианидинов на антиоксидантную активность. Антиоксидантная активность (IC50, мг/л) экстрактов, полученных с использованием органических растворителей, в пересчете на (2,2-дифенил-1-пикрилгидразил) DPPH•, варьировалась от 4,05 до 9,58 в зависимости от температуры в диапазоне от 70 до 150 °C. В то же время результаты, полученные с использованием деионизированной воды, показали многообещающие результаты в диапазоне 6,33–7,36 при температуре от 70 до 150 °C.. Экстракция с помощью деионизированной воды показала, что около 90% веществ, которые извлекаются с помощью органических растворителей путём последовательной экстракции, могут быть получены в виде экстрактов из деионизированной воды.
В исследовании Altınyay et al. [49] были изучены водные и метанольные экстракты A. glutinosa на предмет их ранозаживляющей, противовоспалительной и антиоксидантной активности. Для этого были созданы модели ран in vivo с использованием линейного разреза и кругового иссечения.
Антиоксидантная активность оценивалась с помощью таких методов, как удаление радикалов DPPH и ABTS, снижение мощности и денатурация 2-дезоксирибозы, направленной на неспецифический гидроксильный радикал.
Наиболее эффективный экстракт — метанольный экстракт шишек A. glutinosa — был фракционирован с помощью метода, управляемого биоанализом. Анализы ЯМР и ИК показали, что выделенное соединение представляет собой шикимовую кислоту.
Применение экстрактов A. glutinosa способствовало увеличению натяжения раны на 42,79% и обеспечило сокращение на 51,58%. Наилучшие результаты были достигнуты с использованием фракции EtOAc:MeOH (Fr. D), субфракции D27-38 и шикимовой кислоты.
В анализе проницаемости капилляров, вызванной уксусной кислотой, экстракты MB, Fr. D, субфракция D27-38 и шикимовая кислота продемонстрировали значительные ингибирующие эффекты, составившие 30,22%, 32,46%, 38,24% и 27,19% соответственно.
В модели отека задней лапы, вызванного каррагинаном, экстракт MB также показал хорошие результаты, обеспечив 29,1% ингибирования. Кроме того, субфракция D27-38 и особенно шикимовая кислота проявили выраженные противовоспалительные и антиоксидантные свойства.
Шикимовая кислота продемонстрировала значительный ингибирующий эффект (38,24%) на фермент гиалуронидазу. Результаты исследования позволяют предположить, что шикимовая кислота является основным соединением, ответственным за антиоксидантную активность [49].
Анализ литературы [48, 49] показал, что фенольные соединения, извлечённые из A. glutinosa с помощью экстракции метанолом или этанолом, обладают ярко выраженными антиоксидантными свойствами. Это было подтверждено и в наших исследованиях. Однако водные экстракты A. glutinosa не продемонстрировали значительных антиоксидантных, антибактериальных или противовоспалительных свойств [48].
4. Материалы и методы
4.1. Реагенты
Индивидуальные фенольные компоненты были идентифицированы по характерным временам удерживания и спектрам, которые соответствовали эталонным образцам.. В ходе исследования были использованы следующие аналитические стандарты:
- Кафтаровая кислота (CAS 67879-58-7) — аналитический стандарт
- Хлорогеновая кислота (CAS 327-97-9, ≥95,0%)
- Транс-кофеиновая кислота (CAS 501-16-6) — аналитический стандарт
- П-кумаровая кислота (CAS 501-98-4, ≥98,0%)
- Транс-феруловая кислота (CAS 537-98-4) — аналитический стандарт
- Цикориевая кислота (CAS 6537-80-0, ≥95,0% чистоты для ВЭЖХ)
- Розмариновая кислота (CAS 20283-92-5, 96,0%)
- Апигенин-7-O-глюкозид (CAS 578-74-5, 93,47%)
- Акацетин (CAS 480-44-4, ≥95% чистоты для ВЭЖХ)
- 3,4-дигидроксибензойная кислота (протокатеховая кислота, CAS 99-50-3, ≥97,0%)
- Кверцетин-3-D-глюкозид (CAS 482-35-9, ≥90,0% (ВЭЖХ))
- Лютеолин-7-глюкозид (цинарозид, CAS 5373-11-5) — аналитический стандарт
- Гиперозид (CAS 482-36-0) — аналитический стандарт
- Гидрат рутина (CAS 207671-50-9, ≥98,0%)
- Астрагалин (кемпферол-3-глюкозид, CAS 480-10-4, 92,5%)
- Эллаговая кислота (CAS 476-86-4, ≥95,0% (ВЭЖХ))
- (+)-катехин (CAS 154-23-4), ≥99,0% HPLC-grade) и галловая кислота (CAS 149-91-7, аналитический стандарт).
AG Analytekspert, Москва, Россия, предоставила все стандарты и реагенты, которые соответствуют высочайшим стандартам чистоты и качества.
4.2. Объекты исследования
В нашем исследовании мы сосредоточились на лекарственных растениях, произрастающих в Калининградской области: Filipendula ulmaria и Alnus glutinosa, а также на их экстрактах.
Сбор листьев Filipendula ulmaria и женских серёжек Alnus glutinosa проходил с июня по октябрь 2021 года в разных частях региона. Таксономическая идентичность растительного материала была подтверждена доктором Пунгиным, заведующим гербарием Института живых систем Балтийского федерального университета им. И. Канта, согласно протоколу № 8/2021.
4.3. Экстракция
Для глубокого понимания закономерностей, связанных с вторичными метаболитами растений, из шишек F. ulmaria и A. glutinosa были получены три различных типа экстрактов:
- Метанольный, полученный по методу Сокслета, который длился 6 часов (11 циклов).
- Этилацетатный, также полученный по методу Сокслета (6 часов, 11 циклов).
- Водный, полученный путем мацерации на кипящей водяной бане с обратным холодильником в течение 30 минут. Для A. glutinosa был добавлен дополнительный этап настаивания в течение 10 минут. Затем следовала мацерация на 70% этаноле на кипящей водяной бане в течение 60-90 минут.
4.4. Определение общего выхода экстрактов
Общий выход экстрактов был определен с помощью гравиметрического метода. Полученные экстракты были сконцентрированы в вакуумном роторном испарителе и высушены в сублимационной сушилке Labconco Triad (Labconco, Канзас-Сити, Миссури, США).
4.5. Качественный и количественный анализ фенольных соединений в растительных экстрактах методом ВЭЖХ
Для проведения ОФ-ВЭЖХ анализов был использован хроматограф LC-20AB Shimadzu Prominence (Shimadzu, Киото, Япония), оснащенный бинарным насосом, диодным матричным детектором SPD-M20A (Shimadzu, Киото, Япония) и ОФ-колонкой Zorbax 300SB-C18 4,6 × 250 мм 5 мкм (Agilent, Санта-Клара, Калифорния, США). Разделение проводилось при температуре 40 °C в режиме градиентного элюирования.
В качестве подвижной фазы использовались следующие растворители: элюент A — 0,1% (об./об.) ТФУ в бидистиллированной воде и элюент B — ацетонитрил с трифторуксусной кислотой. Скорость потока была установлена на уровне 1 мл/мин, а УФ-спектроскопия проводилась при длинах волн 254, 280 и 325 нм.
Концентрации отдельных соединений в экстрактах были определены методом внешней стандартизации. Точность данного метода составила от 3 до 7%.
4.6. Определение антиоксидантной активности
Антиоксидантную активность (АОА) растительных экстрактов оценивали по их способности взаимодействовать со свободными радикалами, используя различные методы. Эти методы включали:
- Метод DPPH: Антиоксидантную активность измеряли с помощью 2,2-дифенил-1-пикрилгидразила (DPPH), который реагирует на свободные радикалы, образуя окрашенное соединение. Для определения АОА 20 микролитров растительного экстракта или стандартного раствора смешивали с 300 микролитрами свежеприготовленного 0,1 ммоль/л раствора DPPH. Смесь инкубировали в темноте при комнатной температуре в течение 30 минут. Затем измеряли уменьшение поглощения по сравнению с контролем (используемым растворителем для экстракции) при длине волны 515 нм.
- Метод ABTS: Антиоксидантную активность определяли с помощью 2,2′-азино-бис(3-этилбензотиазолин-6-сульфоновой кислоты (ABTS), которая реагирует на свободные радикалы аналогично DPPH. Для этого 10 микролитров растительного экстракта или стандартного раствора смешивали с 400 микролитрами свежеприготовленного 5 ммоль/л раствора ABTS. Смесь инкубировали в темноте при комнатной температуре в течение 30 минут. Регистрацию уменьшения поглощения по сравнению с контролем (используемый растворитель для экстракции) проводили при длине волны 600 нм.
- Метод FRAP: Антиоксидантную активность также оценивали по снижению мощности комплекса Fe(III)-2.4.6-трипиридил-s-триазина (FRAP) в соответствии с методикой, описанной в [21], с некоторыми модификациями. Для этого 20 микролитров растительного экстракта или стандартного раствора вводили в 300 микролитров свежеприготовленного раствора FRAP, который реагирует на свободные радикалы. Смесь инкубировали в темноте при комнатной температуре в течение 30 минут. Уменьшение мощности комплекса FRAP регистрировали при длине волны 450 нм.
Раствор радикала ABTS готовился непосредственно перед проведением анализа. Чтобы получить этот радикал, смешивались аликвоты раствора ABTS с концентрацией 7,0 ммоль/л и раствора персульфата калия с концентрацией 2,45 ммоль/л. Затем раствор выдерживался в течение 16 часов в темноте при комнатной температуре (RT).
Для начала реакции к 300 мкл приготовленного раствора катион-радикала ABTS+ добавлялось 20 мкл растительного экстракта или стандарта. Поглощение измерялось при 734 нм с помощью спектрофотометра UV-1280 (Shimadzu, Киото, Япония) после инкубации смеси в течение 15 минут при температуре 37 °C в темноте. В качестве холостых использовались реагент ABTS и соответствующий растворитель, используемый для экстракции.
При измерении антиоксидантной активности с использованием методов DPPH, ABTS и FRAP в качестве стандартных растворов применяли растворы Trolox (6-гидрокси-2,5,7,8-тетраметилхроман-2-карбоновой кислоты) с известной концентрацией 0,1 М. Результаты анализов выражали в микромолях эквивалентов Trolox на грамм сухой массы растения (мкмоль TE/г).
Все спектрофотометрические измерения проводились с помощью микропланшетного ридера CLARIOstar (BMG Labtech, Ortenberg, Hesse, Germany).
4.7. Статистический анализ
Данные были подвергнуты дисперсионному анализу (ANOVA) с использованием программы Statistica 10.0 (StatSoft Inc., 2007, США). Значимость наблюдаемых различий оценивали с помощью анализа Post hoc (тест Дункана). Равенство дисперсий извлеченных выборок проверяли с помощью теста Левена. Различия между средними значениями считались значимыми, если доверительный интервал был меньше 5% (p < 0,05).
5.Выводы
Растительные антиоксиданты считаются наиболее подходящими для постоянного терапевтического и диетического использования, поскольку они менее токсичны для человека, чем синтетические антиоксиданты, такие как дибунол, пробукол, цисталит и мексамин, которые, в свою очередь, не обладают таким потенциалом в клинической практике [50].
В этом исследовании наиболее обильными образцами фенольных метаболитов были водно-этанольные экстракты F. ulmaria. Метанольные экстракты также продемонстрировали многообещающие результаты. В метанольном экстракте A. glutinosa была обнаружена самая высокая концентрация эллаговой кислоты, и примерно половина этого количества была выявлена в водном экстракте A. glutinosa. С другой стороны, этилацетатные экстракты обоих растений показали наименьший выход фенольных компонентов.
Было установлено, что экстракты A. glutinosa и F. ulmaria обладают высокой антиоксидантной активностью, при этом экстракты A. glutinosa оказались более активными, чем экстракты F. ulmaria.
Свободнорадикальные процессы приводят к окислительной модификации различных биомолекул, таких как липиды, белки и нуклеиновые кислоты, что, в свою очередь, вызывает повреждение и гибель клеток тканей и органов [50].
Поскольку ослабление механизмов антиоксидантной защиты является ключевым фактором, способствующим усилению свободнорадикальных реакций, одним из важнейших направлений биомедицинских исследований является разработка лекарственных препаратов и биологически активных добавок к пище с антиоксидантными свойствами на основе F. ulmaria и A. glutinosa. Эти препараты могут быть использованы для замедления процессов старения в организме человека.
Эти открытия открывают широкие перспективы для дальнейшего применения экстрактов F. ulmaria и A. glutinosa в качестве источника природных антиоксидантов.
Список литературы
- Zhao, E.; Crimmins, E. Mortality and morbidity in ageing men: Biology, Lifestyle and Environment. Rev. Endocr. Metab. Disord. 2022, 1–21.
- Rodgers, J.L.; Jones, J.; Bolleddu, S.I.; Vanthenapalli, S.; Rodgers, L.E.; Shah, K.; Karia, K.; Panguluri, S.K. Cardiovascular Risks Associated with Gender and Aging. J. Cardiovasc. Dev. Dis. 2019, 6, 19.
- Zeka, K.; Ruparelia, K.; Arroo, R.R.J.; Budriesi, R.; Micucci, M. Flavonoids and Their Metabolites: Prevention in Cardiovascular Diseases and Diabetes. Diseases 2017, 5, 19.
- Smith, R.E.; Tran, K.; Smith, C.C.; McDonald, M.; Shejwalkar, P.; Hara, K. The Role of the Nrf2/ARE Antioxidant System in Preventing Cardiovascular Diseases. Diseases 2016, 4, 34.
- Dal, S.; Sigrist, S. The Protective Effect of Antioxidants Consumption on Diabetes and Vascular Complications. Diseases 2016, 4, 24.
- Li, Y.; Zhang, J.J.; Xu, D.P.; Zhou, T.; Zhou, Y.; Li, S.; Li, H.B. Bioactivities and health benefits of wild fruits. Int. J. Mol. Sci. 2016, 17, 1258.
- Zhang, J.J.; Li, Y.; Zhou, T.; Xu, D.P.; Zhang, P.; Li, S.; Li, H.B. Bioactivities and health benefits of mushrooms mainly from China. Molecules 2016, 21, 938.
- Wojtunik-Kulesza, K.A.; Oniszczuk, A.; Oniszczuk, T.; Waksmundzka-Hajnos, M. The influence of common free radicals and antioxidants on development of Alzheimer’s disease. Biomed. Pharmacother. 2016, 78, 39–49.
- Balmus, I.M.; Ciobica, A.; Trifan, A.; Stanciu, C. The implications of oxidative stress and antioxidant therapies in inflammatory bowel disease: Clinical aspects and animal models. Saudi J. Gastroenterol. 2016, 22, 3–17.
- Prasad, K.N. Simultaneous activation of Nrf2 and elevation of antioxidant compounds for reducing oxidative stress and chronic inflammation in human Alzheimer’s disease. Mech. Ageing Dev. 2016, 153, 41–47.
- Salomone, F.; Godos, J.; Zelber-Sagi, S. Natural antioxidants for non-alcoholic fatty liver disease: Molecular targets and clinical perspectives. Liver Int. 2016, 36, 5–20.
- Zhou, Y.; Li, Y.; Zhou, T.; Zheng, J.; Li, S.; Li, H.B. Dietary natural products for prevention and treatment of liver cancer. Nutrients 2016, 8, 156.
- Zhou, Y.; Zheng, J.; Li, Y.; Xu, D.P.; Li, S.; Chen, Y.M.; Li, H.B. Natural polyphenols for prevention and treatment of cancer. Nutrients 2016, 8, 515.
- Zheng, J.; Zhou, Y.; Li, Y.; Xu, D.P.; Li, S.; Li, H.B. Spices for prevention and treatment of cancers. Nutrients 2016, 8, 495.
- Xu, D.P.; Li, Y.; Meng, X.; Zhou, T.; Zhou, Y.; Zheng, J.; Zhang, J.J.; Li, H.B. Natural Antioxidants in Foods and Medicinal Plants: Extraction, Assessment and Resources. Int. J. Mol. Sci. 2017, 18, 96.
- Tajner-Czopek, A.; Gertchen, M.; Rytel, E.; Kita, A.; Kucharska, A.Z.; Sokół-Łe˛towska, A. Study of Antioxidant Activity of some Medicinal Plants Having High Content of Caffeic Acid Derivatives. Antioxidants 2020, 9, 412.
- Немерешина О.Н.; Гусев Н.Ф.; Суровяткина Т.Н.; Филиппова А.В. Анализ содержания антиоксидантов в надземной части растения Filipendula Ulmaria (L.) Maxim. степной зоны Оренбургской области. Прок. Оренбург. Государственный аграрный. Унив. 2020, 6, 70-76.
- Кароматов И.Я.; Асланова Д.К. Целебные свойства ольхи. Биол. Интегр. Мед. 2017, 5, 63-68.
- Blazics, B.; Papp, I.; Kery, A. LC-MS Qualitative analysis and simultaneous determination of six Filipéndula salicylates with two standards. Chromatographia 2010, 71, 61–67.
- Круглова, М.Ю. Фитохимическое изучение видов рода Filipendula Mill /М.Ю. Круглова. (Rosaceae), произрастающие в России. Защита кандидатской диссертации, Институт общей и экспериментальной биологии Сибирского отделения Российской академии наук, Улан-Удэ, Россия, 28 февраля 2014 г.
- Wilkes, S.; Glasl, H. Isolation, characterization, and systematic significance of 2-pyrone-4,6-dicarboxylic acid in Rosaceae. Phytochemistry 2001, 58, 441–449.
- Okuda, T.; Yoshida, T.; Hatano, T.; Iwasaki, M.; Kubo, M.; Orime, T.; Yoshizaki, M.; Naruhashi, N. Hydrolysable tannins as chemotaxonomic markers in the Rosaceae. Phytochemistry 1992, 31, 3091–3096.
- Papp, I.; Apati, P.; Andrasek, V.; Blazovics, A.; Balazs, L.; Kursinski, A.; Kite, G.C.; Houghton, P.J.; Kery, A. LC-MS analysis of antioxidant plant phenoloids. Chromatographia 2004, 60, 93–97.
- Fecka, I. Qualitative and quantitative determination of hydrolysable tannins and other polyphenols in herbal products from meadowsweet and dog rose. Phytochem. Anal. 2009, 20, 177–188.
- Сайфуллина, Н.А., Кожина, И.С. Состав эфирных масел из цветков Filipéndula ulmaria (L.) Maxim., Filipéndula denudata (Presl.) Fritsch и Filipéndula stepposa Juz/Н.А. Сайгуллина, И.С. Кожина// Биология растений. Ресурсы растений. 1975, 11, 542-544.
- Halkes, S.B.A.; Beukelman, C.J.; Kroes, B.H.; van den Berg, A.J.J.; van Dijk, H.; Labadie, R.P. A strong complement inhibitor from the flowers of Filipéndula ulmaria (L.) Maxim. Pharm. Pharmacol. Lett. 1997, 7, 79–85.
- Barros, L.; Alves, C.T.; Dueñas, M.; Silva, S.; Oliveira, R.; Carvalho, A.M.; Henriques, M.; Santos-Buelga, C.; Ferreira, I.C.F.R. Characterization of phenolic compounds in wild medicinal flowers from Portugal by HPLC-DAD-ESI/MS and evaluation of antifungal properties. Ind. Crop. Prod. 2013, 44, 104–107.
- Nitta, Y.; Kikuzaki, H.; Azuma, T.; Ye, Y.; Sakaue, M.; Higuchi, Y.; Komori, H.; Ueno, H. Inhibitory activity of Filipéndula ulmaria constituents on recombinant human histidine decarboxylase. Food Chem. 2013, 138, 1551–1559.
- Шалабаева, Т.М.; Высочина, Г.И.; Костикова, В.А. Фенольные соединения и антиоксидантная активность некоторых видов рода Filipendula Mill. Булл. сер. ВГУ. Хим.. Биол. Фарм. 2018, 1, с. 204-210.
- Cherpakov, V.V. Bacterioses of black alder (Alnus glutinosa (L.) Gaertn) in the Western Caucasus. Actual Probl. For. Complex 2016, 44, 143–149.
- Labat-Robert, J.; Robert, L. Longevity and aging. Mechanisms and perspectives. Pathol. Biol. 2015, 63, 272–276.
- Rajbhar, K.; Dawda, H.; Mukundan, U. Polyphenols: Methods of extraction. Sci. Revs. Chem. Commun. 2015, 5, 1–6.
- Зыкова, И.Д.; Ефремов, А.А. Компонентный состав эфирного масла из соцветий Filipendula ulmaria (L.) Maxim. в фазах цветения и плодоношения. Хим.. Растительная сырая вода. 2011, 1, 133-136.
- Круглова, Ю.В.; Ханна, М.А. Изучение эфирных масел из надземных частей Filipendula ulmaria (L.) Maxim. Med. Educ. Sib. 2011, 5, 7.
- Бубенчиков В.Н., Сухомлинов Ю.А. Минеральный состав растений рода лабазник. Бык. ВГУ, 2006, 1, с. 189-190.
- Заяц Д. В. Определение содержания дубильных веществ в лабазнике вязолистном, заготовленном на территории Архангельской области // Бюл. Сев. гос. мед. ун-та. 2016. № 1. С. 293–294.
- Hare, D.V. Determination of flavonoids in meadowsweet (Filipendula ulmaria L.) growing on the territory of the Arkhangelsk area. Mod. Sci. Res. Innov. 2016, 4, 614–620.
- Зыкова И.Д., Ефремов А.А., Герасимов В.С. Особенности накопления макро- и микроэлементов в надземной части Filipendula ulmaria (L.) Maxim. в разные фенологические фазы // Хим.-раст. сыр. мат. 2013. Т. 2. С. 189–193.
- Tsugkiev, B.G.; Gagiev, L.C.; Sozanov, T.U.; Karaev, K.G. The content of metals and biologically active substances in the meadowsweet Elm-leaved (Filipendula ulmaria (L.) Maxim.). Proc. Gorsky State Agrar. Univ. 2017, 54, 202–207.
- Harbourne, N.; Marete, E.; Jacquier, J.C.; O’Riordan, D. Effect of drying methods on the phenolic constituents of meadowsweet (Filipendula ulmaria) and willow (Salix alba). LWT-Food Sci. Technol. 2009, 42, 1468–1473.
- Krasnov, E.A.; Raldugin, V.; Shilova, I.V.; Avdeeva, E.Y. Phenolic compounds from Filipendula ulmaria. Chem. Nat. Compd. 2006, 42, 148–151.
- Olennikov, D.N.; Kruglova, M.Y. A new quercetin glycoside and other phenolic compounds from the genus Filipendula Chem. Nat. Compd. 2013, 49, 610–616.
- Rauha, J.P.; Remes, S.; Heinonen, M.; Hopia, A.; Kahkonen, M.; Kujala, T.; Pihlaja, K.; Vuorela, H.; Vuorela, P. Antimicrobial effects of Finnish plant extracts containing flavonoids and other phenolic compounds. Int. J. Food Microbiol. 2000, 56, 3–12.
- Dahija, S.; Cakar, J.; Vidic, D.; Maksimovic´, M.; Paric´, A. Total phenolic and flavonoid contents, antioxidant and antimicrobialˇ activities of Alnus glutinosa (L.) Gaertn., Alnus incana (L.) Moench and Alnus viridis (Chaix) DC extracts. Nat. Prod. Res. 2014, 24, 2317–2320.
- Skrypnik, L.; Novikova, A. Response Surface Modeling and Optimization of Polyphenols Extraction from Apple Pomace Based on Nonionic Emulsifiers. Agronomy 2020, 10, 92.
- Shilova, I.; Krasnov, E.; Korotkova, E.; Nagaev, M.; Lukin, A. Antioxidant properties of extracts from the above-ground parts of Filipendula ulmaria. Pharm. Chem. J. 2006, 40, 660–662.
- Zhang, H.; Li, G.; Han, R.; Zhang, R.; Ma, X.; Wang, M.; Shao, S.; Yan, M.; Zhao, D. Antioxidant, Anti-Inflammatory, and Cytotoxic Properties and Chemical Compositions of Filipendula palmata (Pall.) Maxim. Evid. Based Complement. Altern. Med. 2021, 2021, 6659620.
- Lauberts, M.; Pals, M. Antioxidant Activity of Different Extracts from Black Alder (Alnus glutinosa) Bark with Greener Extraction Alternative. Plants 2021, 10, 2531.
- Altınyay, Ç.; Süntar, I.; Altun, L.; Keles¸, H.; Küpeli Akkol, E. Phytochemical and biological studies on Alnus glutinosa subsp. glutinosa, A. orientalis var. orientalis and A. orientalis var. pubescens leaves. J. Ethnopharmacol. 2016, 4, 148–160.
- Chekhani, N.R.; Teselkin, Y.O.; Pavlova, L.A.; Kozin, S.V.; Lubitsky, O.B. Antioxidant activity of plants used in ethnomedicine of Tuva. Bull. Russ. State Med. Univ. 2012, 6, 66–69.

Добавить комментарий